L’insuffisance ovarienne prématurée — longtemps appelée « ménopause précoce », terme que les recommandations actuelles déconseillent car trop définitif — est une réalité médicale difficile à vivre, annoncée souvent à des femmes jeunes en plein désir de maternité. Elle ne signifie ni stérilité absolue, ni absence de solution, mais elle nécessite une prise en charge globale : hormonale pour protéger la santé, et si nécessaire médicalement assistée pour le projet parental. Les critères diagnostiques ont été mis à jour par l’ESHRE en 2024 — c’est la version de référence que cet article utilise.
Qu’est-ce que l’insuffisance ovarienne prématurée ?
L’IOP (insuffisance ovarienne prématurée — aussi appelée insuffisance ovarienne primitive dans certains contextes) correspond à une perte de la fonction ovarienne avant l’âge de 40 ans. Sur le plan biologique, il s’agit d’un hypogonadisme hypergonadotrope : les ovaires ne répondent plus aux stimulations hormonales de l’hypophyse (FSH et LH élevées), et la production d’estradiol est effondrée. Le stock folliculaire est épuisé ou quasi-épuisé, et les cycles menstruels deviennent irréguliers puis s’arrêtent.
Le terme « ménopause précoce » est progressivement abandonné par la communauté médicale car il peut être trompeur : une IOP n’est pas toujours définitive. Des formes fluctuantes existent, avec des poussées de folliculogenèse spontanée qui expliquent les grossesses non planifiées parfois observées chez ces patientes (3 à 10 % de chances de grossesse spontanée). La fertilité spontanée est très faible mais non nulle — fait important à intégrer dans la prise en charge contraceptive si une grossesse n’est pas souhaitée.
Épidémiologie et facteurs de risque
La prévalence de l’IOP est stable dans le temps selon les données épidémiologiques récentes (étude finlandaise Silvén, 2022). En revanche, la composante héréditaire est significative : une femme dont la mère, sœur ou autre parente au premier degré a développé une IOP a un risque multiplié par 18 par rapport à la population générale. Les formes familiales représentent 15 à 20 % de l’ensemble des IOP. Un bilan génétique familial est justifié dès le diagnostic confirmé, et une information sur le risque d’IOP doit être transmise aux sœurs et à la fille de la patiente.
Le diagnostic : critères ESHRE 2024
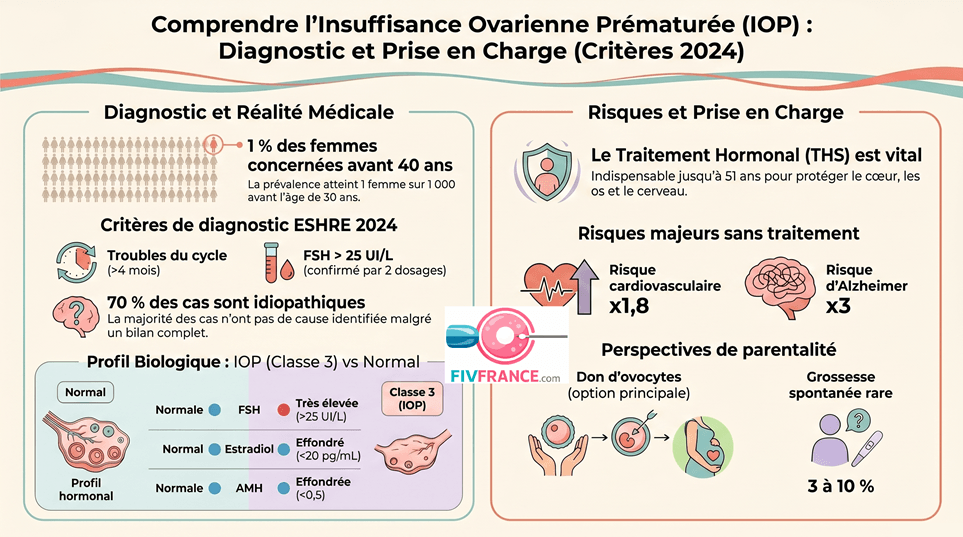
Les critères diagnostiques de l’IOP ont été actualisés par l’ESHRE (European Society of Human Reproduction and Embryology) en 2024. Ils permettent de poser le diagnostic de façon plus précoce et plus fiable.
📋 Critères diagnostiques ESHRE 2024
Note : le diagnostic est posé cliniquement (sans dosage) en cas d’ovariectomie bilatérale avant 40 ans.
Le premier motif de consultation est souvent une aménorrhée secondaire ou une difficulté à concevoir. Les signes d’hypœstrogénie qui accompagnent parfois l’aménorrhée — bouffées de chaleur, sueurs nocturnes, sécheresse vaginale, troubles de l’humeur, baisse de la libido — sont inconstants et parfois absents, surtout dans les formes d’installation progressive.
Classification OMS et profil hormonal
L’IOP correspond à la classe 3 de la classification OMS des troubles de l’ovulation — celle des insuffisances ovariennes. Le tableau biologique et échographique est très caractéristique et permet de la distinguer rapidement des anovulations des classes 1 (origine centrale) et 2 (eugonadotropes, dont le SOPK).
| Paramètre | Normal | Classe 1 | Classe 2 | Classe 3 |
|---|---|---|---|---|
| Follicules antraux (CFA) | Normal | Élevé (petits follicules denses) | Élevé++ (aspect polykystique) | Très bas à absent |
| Estradiol | Normal | Bas | Normal | Effondré |
| FSH | Normale | Basse | Normale | Très élevée >25 UI/L |
| LH | Normale | Basse | Normale à Élevée (SOPK) | Élevée |
| AMH | Normale | Normale à élevée | Normale à très élevée (SOPK) | Effondrée à <0,5 |
Déficit en gonadotrophines (FSH/LH basses). Origine : anorexie, activité physique intense, hyperprolactinémie, syndrome de Kallmann. Traitement : induction par gonadotrophines exogènes ou pompe GnRH.
FSH/LH normales. Cause la plus fréquente : SOPK (rapport LH/FSH >2, AMH très élevée). Traitement : clomifène, létrozole ou gonadotrophines à faibles doses.
Épuisement ou quasi-épuisement du capital folliculaire avant 40 ans. FSH très élevée, estradiol effondré, AMH indétectable. Traitement de la fertilité : don d’ovocytes. THS indispensable.
Les causes de l’IOP
Le bilan étiologique de l’IOP permet d’identifier une cause dans environ 30 % des cas, grâce notamment aux progrès de la génétique. Dans 70 % des cas, aucune cause n’est retrouvée malgré un bilan complet — on parle alors d’IOP idiopathique. La progression des approches génomiques (Plan France Médecine Génomique, séquençage haut-débit) tend à réduire cette proportion en identifiant des variants pathogènes dans des gènes candidats.
- Syndrome de Turner (45,X0)
- Triple X (47,XXX)
- Délétion bras long du X (Xq26–28)
- Prémutation FMR1 (X fragile) — 3–13 % des IOP
- >130 gènes candidats identifiés (PFMG)
- Anticorps anti-ovaire (ABO)
- Maladie d’Addison
- Thyroïdite (Hashimoto)
- Lupus, polyarthrite, Sjögren
- Diabète type 1
- Chimiothérapie (agents alkylants++)
- Radiothérapie pelvienne ou TBI
- Chirurgie ovarienne (kystectomies répétées, endométriose)
- Torsion ovarienne
Formes familiales : 15–20 % des IOP
Risque ischémique ×1,8
Recommandations 2024 (ESHRE)
Déminéralisation osseuse accélérée
Risque fracturaire augmenté
Risque Alzheimer ×3
(annulé si THS jusqu’à 50 ans)
THS jusqu’à 51 ans (âge ménopause physiologique)
Suivi annuel à vie
Conséquences à long terme de la carence estrogénique
L’IOP n’est pas seulement une question de fertilité — c’est une maladie endocrinienne avec des conséquences sur la santé générale qui s’étendent bien au-delà de la sphère reproductive. La carence estrogénique prolongée, si elle n’est pas traitée, expose à des risques significatifs que le THS permet en grande partie de prévenir.
Les recommandations 2024 de l’ESHRE soulignent trois risques principaux : le risque cardiovasculaire ischémique (multiplié par 1,8 sans traitement), le risque d’ostéoporose avec fractures, et un lien épidémiologique avec la maladie d’Alzheimer (risque multiplié par 3, annulé si THS maintenu jusqu’à 50 ans selon les données du CNGOF). Le syndrome génito-urinaire de la ménopause — sécheresse vaginale, dyspareunie, cystites récidivantes — affecte également la qualité de vie et doit être pris en charge.
Le traitement hormonal substitutif (THS) : indispensable
En cas d’IOP, le THS n’est pas une option — c’est une nécessité médicale. Contrairement à la ménopause physiologique de la cinquantaine où le bénéfice-risque du THS est débattu, dans l’IOP le THS protège des risques cardiovasculaire, osseux et neurologique générés par une carence estrogénique anormalement précoce. Il doit être instauré le plus rapidement possible après le diagnostic, et maintenu jusqu’à l’âge physiologique de la ménopause (environ 51 ans).
✅ Modalités du THS dans l’IOP (recommandations ESHRE 2024)
- Estradiol transdermique en première intention (patch, gel) — dose ≥ 100 µg/j ou 1,5–2 mg/j d’estradiol per os
- Associé à une progestérone micronisée orale (schéma combiné séquentiel de préférence pour détecter une grossesse éventuelle)
- Test de grossesse en l’absence d’hémorragie de privation (fertilité spontanée résiduelle)
- Contraception œstroprogestative acceptable si la patiente souhaite aussi une contraception
- Traitement maintenu jusqu’à 51 ans — puis réévaluation comme pour une ménopause physiologique
- Suivi annuel à vie : poids, TA, examen gynécologique, seins, risque cardiovasculaire
IOP et projet parental : les options disponibles
La prise en charge de l’infertilité liée à l’IOP repose sur une réalité difficile à annoncer : les stimulations de l’ovulation sont quasi inopérantes dans ce contexte, car les ovaires ne répondent plus aux gonadotrophines. Les grossesses spontanées sont rares (3 à 10 %) et imprévisibles. Les alternatives doivent être présentées et discutées avec bienveillance, en laissant le temps au couple de traverser les différentes étapes émotionnelles du deuil de la maternité génétique.
🥚 Don d’ovocytes — option principale
La récupération des ovocytes d’une donneuse et la fécondation par le sperme du partenaire permet à la femme de porter elle-même l’enfant. L’utérus des femmes atteintes d’IOP est généralement fonctionnel — les grossesses obtenues par don d’ovocytes sont comparables en termes de suivi obstétrical. En France : prise en charge par l’Assurance Maladie, délais d’attente longs (24 mois en moyenne). Possibilité de se tourner vers des centres espagnols ou belges pour réduire les délais.
🧬 Accueil d’embryon
Embryons issus d’autres couples ayant achevé leur projet parental. Alternative au don d’ovocytes dans certaines situations médicales ou éthiques. Délais d’attente également importants en France.
👶 Adoption
Démarche encadrée par l’Aide Sociale à l’Enfance (ASE) pour les adoptions nationales, et par les organismes autorisés pour les adoptions internationales. Processus long, incertain, mais porteur de projet parental.
❄️ Préservation préventive (avant l’IOP confirmée)
Pour les femmes à risque familial d’IOP ou ayant une réserve ovarienne qui décline rapidement, la congélation d’ovocytes avant que la réserve soit épuisée est la meilleure option. La fenêtre d’action est d’environ 10 ans avant l’IOP confirmée. Une fois l’IOP installée, les ovocytes sont généralement insuffisants pour une congélation.
💙 Accompagnement psychologique — composante essentielle
L’annonce d’une IOP est toujours un choc. La prise en charge psychologique est indissociable du suivi médical. Qu’il s’agisse de traverser le deuil de la maternité génétique, d’envisager les alternatives ou d’accepter « d’apprendre à vivre heureux à deux », l’accompagnement d’un psychologue ou d’une équipe spécialisée est fortement recommandé.
Questions fréquentes sur l’IOP
IOP et ménopause précoce : est-ce la même chose ?
Peut-on tomber enceinte naturellement avec une IOP ?
L’IOP est-elle héréditaire ?
Le THS augmente-t-il le risque de cancer du sein dans l’IOP ?
Qu’est-ce que l’injection de PRP pour l’IOP ?
Sources
📚 Sources et références
- ESHRE (2024). Guidance on premature ovarian insufficiency. Human Reproduction Open. → recomedicales.fr
- HAS. Insuffisance ovarienne prématurée — PNDS. → has-sante.fr
- Réalités en Gynécologie-Obstétrique (nov. 2024). Insuffisance ovarienne prématurée : de nouvelles prises en charge. → realites-gyneco-obstetrique.com
- Plan France Médecine Génomique 2025. Insuffisance ovarienne prématurée et anomalies ovocytaires rares. → pfmg2025.fr
- Dr Benchimol. Insuffisance ovarienne précoce (prématurée). → docteur-benchimol.com
- J. Belaïsh-Allart. Communication FFER 2008 (source originale fivfrance.com).



